
Ventilación en ambientes explosivos I
Hojas Técnicas
Puede resultar útil definir algunos conceptos y exponer los comportamientos de los líquidos, vapores y gases en circunstancias de inflamabilidad y explosión para exponer después el control que puede ejercerse con una ventilación adecuada de las atmósferas conteniendo tales elementos.
Los líquidos en si no son inflamables, son los vapores que de ellos se desprenden los que con aplicación de una llama o chispa provocan el fuego o la explosión. Estos vapores precisan de una determinada proporción de aire y la presencia de una fuente de ignición para entrar en inflamabilidad.
Fig. 1. Explosión
Así, los vapores de la gasolina deben estar presentes de un 1,4% al 7,6% en un volumen de aire para explosionar. Por ello es necesario mantener la gasolina líquida en recipientes estancos y reducir al máximo su contacto con el aire durante su manejo.
Las técnicas de prevención de incendios y explosiones se basan en eliminar las fuentes de ignición, evitar el contacto con el aire, hacer un almacenaje estanco de los líquidos, emplear una atmósfera de gas inerte y usar una ventilación adecuada para diluir las mezclas e impedir concentraciones de gases inflamables.
La gasolina no es el único líquido que emite vapores inflamables a temperatura ambiente. En la tabla del final de la hoja figuran otros muchos líquidos combustibles e inflamables de uso común.
Punto de inflamación, temperatura de ignición, límites de inflamabilidad, índice de evaporación, reactividad al calor, densidad, índice de difusión, amén de otros factores deben tenerse en cuenta para una correcta evaluación del riesgo a que estamos expuestos. Cuando el incendio se ha declarado o la explosión se ha provocado, todos estos factores pierden importancia y el control del siniestro pasa a otro nivel.

Fig.2. Gas metano + aire
1. Clasificación
La asociación americana NFPA define un líquido como un fluido con una presión de vapor inferior a 172 kPa a 38 ºC. Otra clasificación establece tres categorías de líquidos inflamables esquematizados en las tablas 1 y 2.
Muchos productos combustibles son sólidos a temperatura de 38 ºC o más pero al calentarse se transforman en líquidos que emiten vapores inflamables. Ceras, pulimentos, etc. deben considerarse bajo el punto de vista de los líquidos y vapores a que dan lugar al calentarse.
2. Atmósfera explosiva
Es toda mezcla de aire, en condiciones atmosféricas, de sustancias inflamables en forma de gas, vapor, niebla o polvo en las que tras una ignición, la combustión se propaga a la totalidad de la mezcla no quemada. (Definición contenida en la Directiva 94/9/CE).
La temperatura de inflamación está definida por ensayos normalizados según CEI-79-4. El factor tiempo influye también poderosamente como puede colegirse de la Fig. 3 del metano (grisú de las minas).
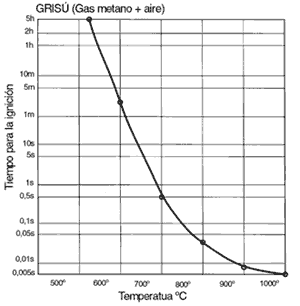
Fig. 3. Grisú (Gas metano + aire)
La energía mínima de inflamación expresada en mJ (mili julios) se indica como ejemplo en la tabla 3.
3. Atmósfera potencialmente explosiva
Se la llama así cuando el riesgo sólo existe en estado potencial, esto es, que la atmósfera pueda derivar a explosiva debido a condiciones locales y de funcionamiento.
4. Punto de inflamación de un líquido
Corresponde a la temperatura más baja a la que la presión de vapor del líquido puede producir una mezcla inflamable en el límite inferior de inflamabilidad. Más sencillo: sin vapor no hay inflamación. Cuanto más temperatura más vapor. Hay una temperatura mínima a la que hay suficiente vapor para inflamar. Es el Punto de Inflamación.
Existen aparatos normalizados para realizar los ensayos que determinan este punto.
5. Temperatura de autoignición de un líquido
Es la temperatura a la que debe calentarse un líquido para que entre en ignición espontánea y arder.
También está normalizado el método para determinar esta temperatura.
En general la temperatura de ignición disminuye al aumentar el peso molecular del líquido. Como ejemplo puede verse la Fig. 4.

Fig. 4. Gráfica de ignición
6. Límites de explosividad
Se define el "Limite Inferior de Explosividad" LIE, como aquel en que la concentración mínima de vapor-aire por debajo de la cual el fuego no se propaga.
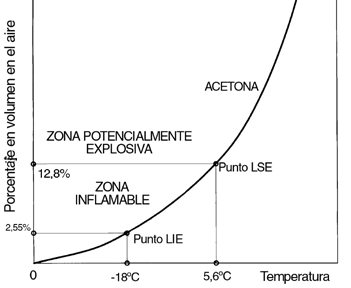
Fig. 5. Gráfica del LIE
Y el "Límite Superior de Explosividad" LSE, como la máxima concentración de vapor-aire por encima de la cual el fuego no se propaga.
Por debajo del LIE se considera que la mezcla es "demasiado pobre" para arder y por encima del LSE es "demasiado rica" también para arder. En este caso, tratándose de motores de explosión, decimos que se "ahoga".
Los límites de explosividad vienen fuertemente influidos por la temperatura y la presión a que está sometido el líquido inflamable. Los vapores que flotan sobre un líquido se reducen al aumentar la presión que se opone a la vaporización y aumentan cuando desciende esta presión. También, a mayor temperatura el líquido tendrá mayor presión de vapor y tenderá a evaporarse en mayores cantidades. El punto de equilibrio sólo puede alcanzarse obviamente en sistemas cerrados como en tanques, tuberías, etc. Al aire libre el líquido vaporizable continuaría evaporándose hasta su total agotamiento.
7. Energía necesaria para la ignición de vapores
Las fuentes de ignición pueden ser muy diversas.
8. Por compresión
Pueden provocarse explosiones muy destructivas a menos que estén controladas y dirigidas, como es el caso dentro de los cilindros de los motores Diesel, en donde la compresión rápida de una mezcla inflamable, de gasoil, genera el calor suficiente hasta su punto de ignición.
La tabla siguiente contiene una lista de productos con indicación de sus características físicas y los límites de explosividad LIE y LSE. También se expresa el MAC, la máxima concentración aceptable para la vida de los humanos. Es un dato muy necesario al tratar de las atmósferas de recintos cerrados, naves o armarios en procesos industriales en los que exista la presencia humana ya que la ventilación de una atmósfera para asegurar su nulo riesgo de explosión puede no ser suficiente para la salud de los ocupantes.
En la segunda parte de esta Hoja Técnica, Ventilación en Ambientes Explosivos II, se darán las fórmulas para calcular la aportación de aire que asegure mantener la atmósfera por debajo del LIE.

Los líquidos en si no son inflamables, son los vapores que de ellos se desprenden los que con aplicación de una llama o chispa provocan el fuego o la explosión. Estos vapores precisan de una determinada proporción de aire y la presencia de una fuente de ignición para entrar en inflamabilidad.
Fig. 1. Explosión
Así, los vapores de la gasolina deben estar presentes de un 1,4% al 7,6% en un volumen de aire para explosionar. Por ello es necesario mantener la gasolina líquida en recipientes estancos y reducir al máximo su contacto con el aire durante su manejo.
Las técnicas de prevención de incendios y explosiones se basan en eliminar las fuentes de ignición, evitar el contacto con el aire, hacer un almacenaje estanco de los líquidos, emplear una atmósfera de gas inerte y usar una ventilación adecuada para diluir las mezclas e impedir concentraciones de gases inflamables.
La gasolina no es el único líquido que emite vapores inflamables a temperatura ambiente. En la tabla del final de la hoja figuran otros muchos líquidos combustibles e inflamables de uso común.
Punto de inflamación, temperatura de ignición, límites de inflamabilidad, índice de evaporación, reactividad al calor, densidad, índice de difusión, amén de otros factores deben tenerse en cuenta para una correcta evaluación del riesgo a que estamos expuestos. Cuando el incendio se ha declarado o la explosión se ha provocado, todos estos factores pierden importancia y el control del siniestro pasa a otro nivel.

Fig.2. Gas metano + aire
1. Clasificación
La asociación americana NFPA define un líquido como un fluido con una presión de vapor inferior a 172 kPa a 38 ºC. Otra clasificación establece tres categorías de líquidos inflamables esquematizados en las tablas 1 y 2.
|
||||||||||||||||||
| Tabla 1. Líquidos inflamables | ||||||||||||||||||
|
|||||||||||||||||
| Tabla 2. Líquidos combustibles | |||||||||||||||||
Muchos productos combustibles son sólidos a temperatura de 38 ºC o más pero al calentarse se transforman en líquidos que emiten vapores inflamables. Ceras, pulimentos, etc. deben considerarse bajo el punto de vista de los líquidos y vapores a que dan lugar al calentarse.
2. Atmósfera explosiva
Es toda mezcla de aire, en condiciones atmosféricas, de sustancias inflamables en forma de gas, vapor, niebla o polvo en las que tras una ignición, la combustión se propaga a la totalidad de la mezcla no quemada. (Definición contenida en la Directiva 94/9/CE).
La temperatura de inflamación está definida por ensayos normalizados según CEI-79-4. El factor tiempo influye también poderosamente como puede colegirse de la Fig. 3 del metano (grisú de las minas).

Fig. 3. Grisú (Gas metano + aire)
La energía mínima de inflamación expresada en mJ (mili julios) se indica como ejemplo en la tabla 3.
|
||||||||||||||||||||||||
| Tabla 3. Líquidos inflamables | ||||||||||||||||||||||||
3. Atmósfera potencialmente explosiva
Se la llama así cuando el riesgo sólo existe en estado potencial, esto es, que la atmósfera pueda derivar a explosiva debido a condiciones locales y de funcionamiento.
4. Punto de inflamación de un líquido
Corresponde a la temperatura más baja a la que la presión de vapor del líquido puede producir una mezcla inflamable en el límite inferior de inflamabilidad. Más sencillo: sin vapor no hay inflamación. Cuanto más temperatura más vapor. Hay una temperatura mínima a la que hay suficiente vapor para inflamar. Es el Punto de Inflamación.
Existen aparatos normalizados para realizar los ensayos que determinan este punto.
5. Temperatura de autoignición de un líquido
Es la temperatura a la que debe calentarse un líquido para que entre en ignición espontánea y arder.
También está normalizado el método para determinar esta temperatura.
En general la temperatura de ignición disminuye al aumentar el peso molecular del líquido. Como ejemplo puede verse la Fig. 4.

Fig. 4. Gráfica de ignición
6. Límites de explosividad
Se define el "Limite Inferior de Explosividad" LIE, como aquel en que la concentración mínima de vapor-aire por debajo de la cual el fuego no se propaga.

Fig. 5. Gráfica del LIE
Y el "Límite Superior de Explosividad" LSE, como la máxima concentración de vapor-aire por encima de la cual el fuego no se propaga.
Por debajo del LIE se considera que la mezcla es "demasiado pobre" para arder y por encima del LSE es "demasiado rica" también para arder. En este caso, tratándose de motores de explosión, decimos que se "ahoga".
Los límites de explosividad vienen fuertemente influidos por la temperatura y la presión a que está sometido el líquido inflamable. Los vapores que flotan sobre un líquido se reducen al aumentar la presión que se opone a la vaporización y aumentan cuando desciende esta presión. También, a mayor temperatura el líquido tendrá mayor presión de vapor y tenderá a evaporarse en mayores cantidades. El punto de equilibrio sólo puede alcanzarse obviamente en sistemas cerrados como en tanques, tuberías, etc. Al aire libre el líquido vaporizable continuaría evaporándose hasta su total agotamiento.
7. Energía necesaria para la ignición de vapores
Las fuentes de ignición pueden ser muy diversas.
• Calor
Producido por rozamientos en máquinas con funcionamiento anormal, desgastes, roturas, etc. Las superficies calientes, deben tener dimensiones y temperatura suficientes para poder inflamar.
• Llamas
Que sean capaces de calentar el vapor hasta la temperatura de ignición de la mezcla.
• Chispas
Las producidas por fricción, de corta duración, pueden no llegar a inflamar mezclas. Las chispas eléctricas, en cambio, sí que suelen tienen energía suficiente y son capaces de producir ignición de las mezclas inflamables.
8. Por compresión
Pueden provocarse explosiones muy destructivas a menos que estén controladas y dirigidas, como es el caso dentro de los cilindros de los motores Diesel, en donde la compresión rápida de una mezcla inflamable, de gasoil, genera el calor suficiente hasta su punto de ignición.
La tabla siguiente contiene una lista de productos con indicación de sus características físicas y los límites de explosividad LIE y LSE. También se expresa el MAC, la máxima concentración aceptable para la vida de los humanos. Es un dato muy necesario al tratar de las atmósferas de recintos cerrados, naves o armarios en procesos industriales en los que exista la presencia humana ya que la ventilación de una atmósfera para asegurar su nulo riesgo de explosión puede no ser suficiente para la salud de los ocupantes.
En la segunda parte de esta Hoja Técnica, Ventilación en Ambientes Explosivos II, se darán las fórmulas para calcular la aportación de aire que asegure mantener la atmósfera por debajo del LIE.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla 4. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 Extractores de baño
Extractores de baño Ventiladores en línea
Ventiladores en línea Extractores para Cristal o Pared
Extractores para Cristal o Pared VMC
VMC Cajas de Ventilación
Cajas de Ventilación Ventiladores de tejado
Ventiladores de tejado Recuperadores de Calor
Recuperadores de Calor Extractores de cocina
Extractores de cocina Campanas y grupos para cocinas
Campanas y grupos para cocinas Ventiladores de confort
Ventiladores de confort Tratamiento de aire
Tratamiento de aire Calefacción de instalación
Calefacción de instalación Calefacción doméstica portatil
Calefacción doméstica portatil Unidades de tratamiento de aire
Unidades de tratamiento de aire Ventiladores helicoidales tubulares
Ventiladores helicoidales tubulares Recuperadores de Calor
Recuperadores de Calor Ventiladores de confort
Ventiladores de confort Secamanos y Secadores de cabello
Secamanos y Secadores de cabello Ventiladores helicoidales murales
Ventiladores helicoidales murales Ventiladores Centrífugos
Ventiladores Centrífugos Extractores desenfumage
Extractores desenfumage Ventilación de parkings
Ventilación de parkings Extractores para atmósferas explosivas ATEX
Extractores para atmósferas explosivas ATEX Cortinas de aire
Cortinas de aire Calefacción industrial
Calefacción industrial Rodete álabes curvados hacia atrás
Rodete álabes curvados hacia atrás Rodete de álabes curvados hacia atrás de alta presión
Rodete de álabes curvados hacia atrás de alta presión Rodete de álabes curvados hacia adelante
Rodete de álabes curvados hacia adelante Rodete de álabes curvados hacia adelante (multipala)
Rodete de álabes curvados hacia adelante (multipala) Rodete de álabes curvados hacia atrás de doble aspiración
Rodete de álabes curvados hacia atrás de doble aspiración Rodete álabes radiales para transporte de materia
Rodete álabes radiales para transporte de materia Ventiladores centrífugos para hornos
Ventiladores centrífugos para hornos Ventiladores helicoidales
Ventiladores helicoidales Accesorios de montaje
Accesorios de montaje Accesorios eléctricos
Accesorios eléctricos

